파이로젠 테스트
파이로젠 검사는 비경구 의약품 및 의료 기기의 안전성에 중요한 검사입니다. 발열을 일으키는 물질로 인해 생명을 잃을 수도 있기 때문에, 파이로젠 검사는 출시전 검사로 필수적입니다. 단핵구 활성 검사(MAT)는 한 번의 생체외 검사로 내독소 및 비내독소 파이로젠 모두를 검출할 수 있는 검사 기법입니다.
섹션 개요
단핵구 활성 검사(MAT)
의약품 및 의료 기기와 같은 비경구 제품에서 내독소 및 비내독소 파이로젠을 검출하기 위해, MAT는 윤리 규정 준수에 따라 동물 실험을 대체할 생체외 검사법도 제공합니다.
토끼 파이로젠 검사와 투구게 변형세포 용해질(LAL) 검사는 파이로젠 검출에 널리 사용됩니다. 두 방법은 모두 동물을 이용하며 일부 제약이 있습니다. 토끼 파이로젠 검사는 동물의 반응이 인간의 반응과 크게 차이를 보일 수 있기 때문에 완건성이 부족함을 보여줍니다. LAL 검사에서는 검사한 시료에 존재할 수 있는 비내독소 파이로젠은 무시하고 내독소만 감지하여 안전 위험을 초래합니다.
이런 제약을 극복하기 위해 2010년 유럽 약전은 토끼 파이로젠 검사(유럽 약전 제2.6.30장)를 대체하는 공정서 기법으로 단핵구 활성 검사(MAT)를 소개했으며 FDA 산업지침에도 기재되었습니다.
주의: 유럽 약전 위원회는 MAT 검사가 최선의 대안이라는 점을 고려하여 3R 원칙에 따라 토끼 파이로젠 검사를 폐지하기로 결정했습니다.
이에 따른 조치를 시작하기 위해 기사를 읽고 자사의 전문가와 더 자세히 논의하십시오.

내독소 및 비내독소 파이로젠 검출을 위한 PyroMAT® 생체외 검사
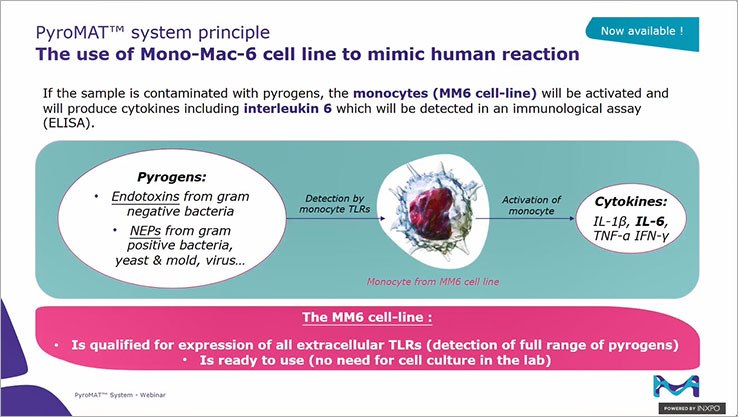
PyroMAT® 시스템은 Mono-Mac-6 세포주와 IL-6 판독을 기반으로 하여 단핵구 활성 검사의 장점과 세포주 사용의 장점을 모두 합친 결과를 제공합니다.
- 광범위한 파이로젠 검출: 알려진 모든 파이로젠을 검출할 수 있어 환자 안전을 보장합니다. 토끼 파이로젠 검사(RPT)와 마찬가지로 MAT는 내독소 및 비내독소 파이로젠 모두를 효과적으로 검출할 수 있습니다.
- 검사할 수 있는 제품 범위 확장: RPT, 박테리아 내독소 검사(BET) 및 LAL과 같이 가장 흔하게 사용되는 기법들은 적용 가능한 제품 유형에 제한이 있지만, MAT는 기법의 적용에 더 많은 유연성을 제공합니다.
- 인간 면역 반응을 모방한 생체외 분석: 동물 생명의 소비를 줄일 수 있는 강력한 예측 모델을 위한 방법입니다.
- 국제 규제 및 지침 준수: 업계와 규제 당국의 윤리 규범을 준수하여 동물 실험을 줄일 수 있습니다.
- 표준화된 반응성과 고감도(LOD 0.05 EU/mL). 세포주를 간편하게 즉시 사용할 수 있어 세포 배양 자체의 필요성을 줄이고, 힘겨운 실험실 작업도 줄일 수 있습니다.
- 인증된 세포: Mono-Mac-6 세포는 MAT의 국제적 검증에서 인용될 뿐만 아니라 광범위한 파이로젠 검출을 보장하는 모든 표면의 Toll-Like Receptors (TLRs) 발현을 인증받았습니다.
비내독소 파이로젠 양성 대조군에 대해 자세히 알아보십시오.
비내독소 파이로젠 양성 대조군
유럽 약전의 챕터 2.6.30(단핵구 활성 검사)에 따르면 “톨형 수용체를 위해 최소 두 개의 비내독소 리간드를 준비 검사에 포함할 것[이하 생략]과 다음 사항을 요청하고 있습니다. 사용되는 비내독소 파이로젠의 선택은 검사 중인 물질 중 가장 높은 오염물을 가진 것으로 반영해야 합니다.”
이러한 요구에 대응하기 위해 당사는 다음과 같은 다양한 양성 대조군을 제공하고 있습니다.
- 일반적으로 의약품 생산 공정에서 발견되는 여러 유형의 오염물질(그램 음성 및 그램 양성균, 바이러스 및 마이코플라스마)을 반영합니다.
- 여러 단핵성 톨형 수용체(TLR) 표적화
리간드 | 표적 TLR | 반영된 오염물질 유형 |
|---|---|---|
HKSA | TLR2 | 그램 양성균 |
플라젤린 | TLR5 | 그램 양성 및 그램 음성균 |
PAM3CSK4 | TLR2/1 | 그램 양성 및 그램 음성균 |
Resiquimod | TLR7/8 | 바이러스 |
FSL1 | TLR2/6 | 마이코플라스마 |
비내독소 파이로젠 양성 대조군에 대해 자세히 알아보십시오.

- 광범위한 파이로젠 검출: 토끼 발열 검사(RPT)와 마찬가지로 MAT는 내독소와 NEP를 모두 검출합니다.
- 검사할 수 있는 제품 범위 확장: RPT, 박테리아 내독소 검사(BET) 및 LAL과 같이 가장 흔하게 사용되는 기법들은 적용 가능한 제품 유형에 제한이 있지만, MAT는 기법의 적용에 더 많은 유연성을 제공합니다.
- 인간 면역 반응을 모방한 생체외 분석: 동물 생명의 소비를 줄일 수 있는 강력한 예측 모델을 위한 방법입니다.
- 국제 규제 및 지침 준수: 업계와 규제 당국의 윤리 규범을 준수하여 동물 실험을 줄일 수 있습니다.
- 8인의 기증자로부터 수집한 냉동보존 혈액: 파이로젠에 대한 인간의 면역 반응과 최대한 유사한 결과를 낼 수 있습니다.
자사에서 제공하는 아래의 서비스를 활용하여 간편한 검증과 비용 효율적인 검사를 위해 파이로젠 검사법을 최적화 또는 단순화할 수 있습니다.
- 적용 서비스
- 검증 서비스
- 교육 서비스
토끼, LAL 및 MAT의 파이로젠 검사 비교 | |||||
|---|---|---|---|---|---|
| 토끼 | LAL | MAT (PyroDetect System) | MAT (PyroMAT® System) | ||
| 검사 유형 | 생체내 | 탈체 | 생체외(냉동보존 전혈) | 생체외(단핵구 세포주) | |
| 동물 소비 | ++ | + | - | - | |
| 오염 검출 | 내독소(예: 그람 음성균에서 검출되는 LPS) | + | + | + | + |
| 그람 양성(LTA) | + | - | + | + | |
| 진균 | + | - | + | + | |
| 세균 | +/- | - | + | + | |
| 적용 분야 | 제약품 | + | + | + | + |
| 생물학 | + | +/- | + | + | |
| 의료 기기 | + | +/- | + | + | |
| 세포 요법 | - | +/- | + | + | |
MAT 구현 및 검증을 위한 자료 부족. 저희가 해결해드립니다!
파이로젠 검사 구현을 지원하기 위한 타당성 연구, 검증법 개발, 검증 및 교육 서비스에 대해 자사의 파이로젠 검사 전문가와 상담하십시오.
관련 제품 자료
- Brochure: PyroMAT® and PyroDetect
Used to detect a broad range of pyrogens in parenteral products such as pharmaceuticals, biopharmaceuticals or medical devices, the MAT gives an in vitro alternative to conventional animal testing in accordance with regulatory guidelines.
- Article: Pyrogen Contamination Risk by Dr. Tim Sandle
Unlike the LAL test, the MAT is a powerful in vitro test for the detection of both endotoxin and non-endotoxin pyrogens (NEPs) acting via the toll-like receptors (TLRs) pathway.
- Data Sheet: Validation Method - PyroMAT® System
The Monocyte Activation Test (MAT) was introduced in the European Pharmacopeia (Chapter 2.6.30) in 2010, as a compendial method that can be used to replace the Rabbit Pyrogen Test (RPT).
- Infographic: MAT Implementation Workflow
Implementation of our Monocyte Activation Test (MAT), the PyroMAT® system.
- Poster: Pyrogen Detection in Pharma QC: Moving Away from the RPT
We have demonstrated that the MM6 cells are suitable for the detection of various NEPs targeting different monocytic toll-like receptors, making MM6 cell line-based MAT suitable for RPT replacement.
- Application Note: Detection of NEP by MAT Using the PyroMAT® System
The monocyte activation test (MAT) is the human in vitro alternative to the rabbit pyrogen test, and allows the detection of the full range of pyrogens, including endotoxins and non-endotoxin pyrogens (NEPs).
- Application Note: Detection of Pyrogens in Vaccines with PyroMAT® System
The PyroMAT® System uses cryo-preserved Mono-Mac-6 (MM6) human monocytic cells as a source of monocytes. The response to pyrogenic substances is determined by measurement of Interleukin-6 (IL-6) produced by the MonoMac 6 cells.
- Questions & Answers about MAT. Dr. Tim Sandle Reponds
Risk considerations for the presence of pyrogens and the need for the MAT test in pharmaceutical processing.
- White Paper: Monocyte Activation Test
In this context, the in vitro pyrogen test based on human cells offers a valuable alternative to the rabbit pyrogen test.
- Application Note: Detection of Pyrogens in Hormone-based Drugs
For the quantification of the pyrogenic load of a sample, method A in accordance with the European Pharmacopeia can be conducted.
- Application Note: Detection of Pyrogens in FBS with PyroMAT® System
The response to pyrogenic substances is determined by measurement of Interleukin-6 (IL-6) produced by the Mono-Mac-6 cells. For this purpose, the ELISA-microplate supplied in the kit is coated with an antibody specific to IL-6.
계속 읽으시려면 로그인하거나 계정을 생성하세요.
계정이 없으십니까?