おすすめの製品
生物化学的/生理学的作用
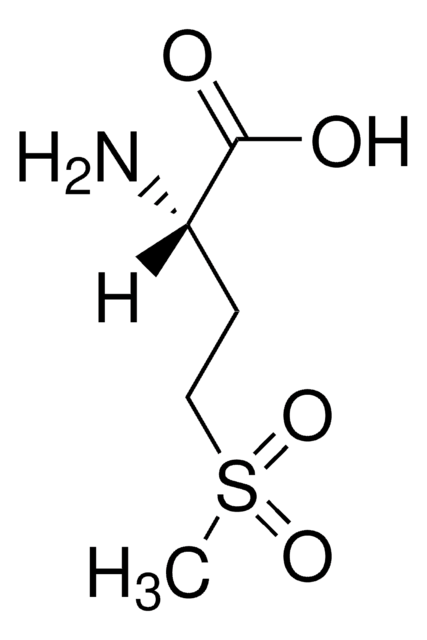
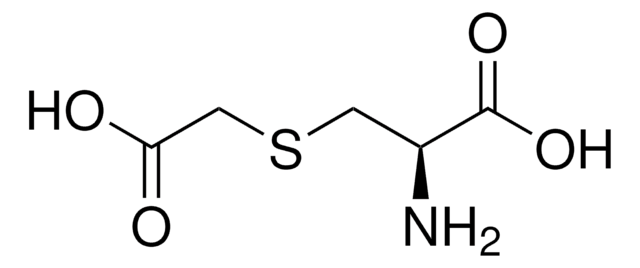
L-システインS-硫酸塩(LCSS)はNMDA グルタミン酸作動性受容体作動薬として使用されます。LCSSはシスチン付加酵素の基質として働きます。
システインは成長、繁殖、保存および免疫と関連する機能的なアミノ酸の1つです。システインはタンパク質のジスルフィド結合の源であって、硫黄の輸送と関連しています。生理的pHにおいて、システインは急速酸化を受けてシスチンが生成されます。システインあるいはシスチンの有効性の低下は白血球の代謝に影響を与えます。 L-システインはニューロンで起こるグルタチオン合成における律速段階の場合の前駆体として働きます。L-システインは解毒反応に無機硫酸塩を提供します。そのため、L-システインは神経保護と関連している可能性があります。L-システインは重金属イオンが血液脳関門を越えて脳中に移行することを妨げることが明らかになっています。L-システインのレベルが増大すると神経毒性がもたらされる可能性があります。
システインは成長、繁殖、保存および免疫と関連する機能的なアミノ酸の1つです。システインはタンパク質のジスルフィド結合の源であって、硫黄の輸送と関連しています。生理的pHにおいて、システインは急速酸化を受けてシスチンが生成されます。システインあるいはシスチンの有効性の低下は白血球の代謝に影響を与えます。 L-システインはニューロンで起こるグルタチオン合成における律速段階の場合の前駆体として働きます。L-システインは解毒反応に無機硫酸塩を提供します。そのため、L-システインは神経保護と関連している可能性があります。L-システインは重金属イオンが血液脳関門を越えて脳中に移行することを妨げることが明らかになっています。L-システインのレベルが増大すると神経毒性がもたらされる可能性があります。
シグナルワード
Warning
危険有害性情報
危険有害性の分類
Eye Irrit. 2 - Skin Irrit. 2 - STOT SE 3
ターゲットの組織
Respiratory system
保管分類コード
11 - Combustible Solids
WGK
WGK 3
引火点(°F)
Not applicable
引火点(℃)
Not applicable
個人用保護具 (PPE)
dust mask type N95 (US), Eyeshields, Gloves
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
C2196-5MG:
C2196-VAR:
C2196-25MG:
C2196-25MG-PW:
C2196-BULK:
C2196-5MG-PW:
最新バージョンのいずれかを選択してください:
試験成績書(COA)
Lot/Batch Number
この製品を見ている人はこちらもチェック
Desensitization of NMDA receptor channels is modulated by glutamate agonists.
Nahum-Levy R
Biophysical Journal, 80(5), 2152-2166 (2001)
Takeshi Nakatani et al.
Microbial cell factories, 11, 62-62 (2012-05-23)
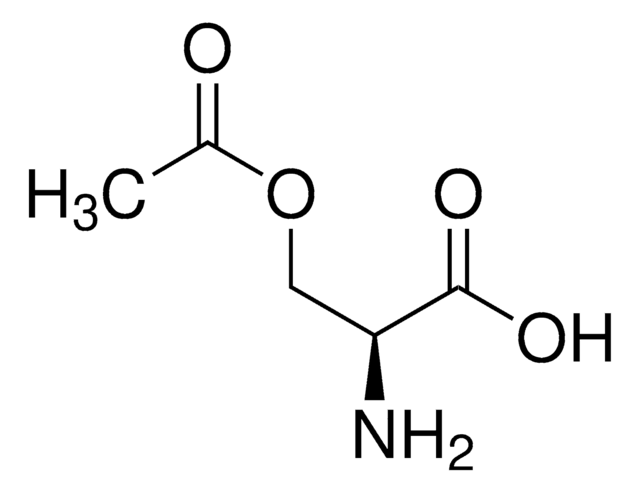
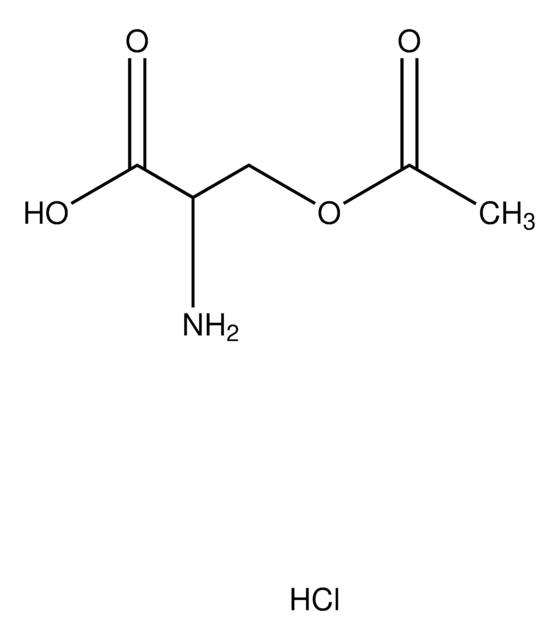
Escherichia coli has two L-cysteine biosynthetic pathways; one is synthesized from O-acetyl L-serine (OAS) and sulfate by L-cysteine synthase (CysK), and another is produced via S-sulfocysteine (SSC) from OAS and thiosulfate by SSC synthase (CysM). SSC is converted into L-cysteine
E C Ramírez et al.
Journal of agricultural and food chemistry, 47(6), 2218-2225 (2000-05-04)
Cystine lyase is the enzyme responsible for off-aroma deterioration in fresh unblanched broccoli. In this research, cystine lyase purification from broccoli has been optimized. Only one protein peak with cystine lyase activity was found during purification. Broccoli cystine lyase was
R Nahum-Levy et al.
Biophysical journal, 80(5), 2152-2166 (2001-04-28)
Two distinct forms of desensitization have been characterized for N-methyl-D-aspartate (NMDA) receptors. One form results from a weakening of agonist affinity when channels are activated whereas the other form of desensitization results when channels enter a long-lived nonconducting state. A
Cecilia Gotor et al.
Plant signaling & behavior, 5(8), 1028-1030 (2010-08-12)
The cysteine molecule plays an essential role in cells because it is part of proteins and because it functions as a reduced sulfur donor molecule. In addition, the cysteine molecule may also play a role in the redox signaling of
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)