おすすめの製品
製品名
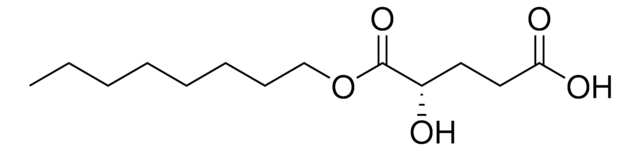
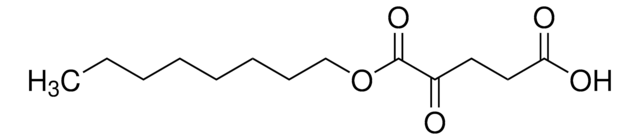
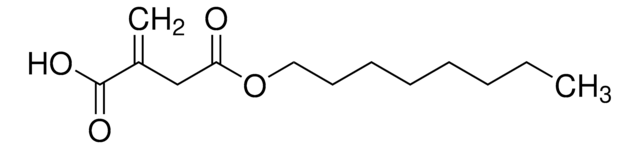
オクチル-(R)-2HG, ≥98% (HPLC)
アッセイ
≥98% (HPLC)
フォーム
film
保管条件
desiccated
色
colorless
溶解性
DMSO: 2 mg/mL, clear
保管温度
−20°C
SMILES記法
O[C@H](CCC(=O)O)C(=O)OCCCCCCCC
InChI Key
UJZOKTKSGUOCCM-LLVKDONJSA-N
アプリケーション
オクチル-(R)-2ヒドロキシグルタレート(HG)は、NANOG転写因子の発現に対する影響を検討するための膠芽腫細胞の膜透過性オンコメタボライトとして用いられています。また、酵素α-ケトグルタル酸(α-KG)依存性デオキシゲナーゼの競合的阻害剤としても用いられています。
生物化学的/生理学的作用
オクチル-(R)-2HG(オクチル-D-2HG)は、NADP+-依存性イソクエン酸デヒドロゲナーゼ遺伝子IDH1およびIDH2の変異により腫瘍細胞で産生される、がん代謝物D-2-ヒドロキシグルタル酸(D-2HG)の細胞膜透過前駆体型です。D-2HGは、α-KG結合と競合することにより、複数のα-ケトグルタル酸/α-KG依存性ジオキシゲナーゼを阻害します。オクチル-(R)-2HG処理(1~50 mM)による細胞内D-2HGの放出は、α-KG依存性ジオキシゲナーゼプロリルヒドロキシラーゼ(PHD)およびコラーゲンプロリル-4-ヒドロキシラーゼ(C-P4H)をそれぞれ阻害した結果、デメチラーゼ活性を抑制し(約148%H3K9me2および約310% H3K79me2増加; 50 mM /U-87MG)、HIF-1αを増加させ、エンドスタチン濃度を減少させることが示されています。
調製ノート
The density is not reported for this compound. The molecular weight is 260.33. The solubility is tested at 2mg/mL in DMSO, however other sources suggest that it is soluble in DMSO up to 10mg/mL.
保管分類コード
11 - Combustible Solids
WGK
WGK 3
引火点(°F)
Not applicable
引火点(℃)
Not applicable
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
SML2200-25MG:
SML2200-5MG:
SML2200-BULK:
SML2200-VAR:
最新バージョンのいずれかを選択してください:
試験成績書(COA)
Lot/Batch Number
この製品を見ている人はこちらもチェック
Zachary J Reitman et al.
The Journal of biological chemistry, 289(34), 23318-23328 (2014-07-06)
Mutations in the cytosolic NADP(+)-dependent isocitrate dehydrogenase (IDH1) occur in several types of cancer, and altered cellular metabolism associated with IDH1 mutations presents unique therapeutic opportunities. By altering IDH1, these mutations target a critical step in reductive glutamine metabolism, the
alpha-Ketoglutarate-Activated NF-$\kappa$B Signaling Promotes Compensatory Glucose Uptake and Brain Tumor Development
Wang X, et al.
Molecular Cell, 76(1), 148-162 (2019)
IDH1R132H Causes Resistance to HDAC Inhibitors by Increasing NANOG in Glioblastoma Cells
Kim G H, et al.
International Journal of Molecular Sciences, 20(11), 2679-2679 (2019)
Parker L Sulkowski et al.
Science translational medicine, 9(375) (2017-02-06)
2-Hydroxyglutarate (2HG) exists as two enantiomers, (R)-2HG and (S)-2HG, and both are implicated in tumor progression via their inhibitory effects on α-ketoglutarate (αKG)-dependent dioxygenases. The former is an oncometabolite that is induced by the neomorphic activity conferred by isocitrate dehydrogenase
Jing-Yi Chen et al.
Scientific reports, 6, 32428-32428 (2016-09-01)
Mutations of isocitrate dehydrogenase 1 (IDH1) and IDH2 in acute myeloid leukemia (AML) cells produce the oncometabolite R-2-hydroxyglutarate (R-2HG) to induce epigenetic alteration and block hematopoietic differentiation. However, the effect of R-2HG released by IDH-mutated AML cells on the bone
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)