おすすめの製品
製品名
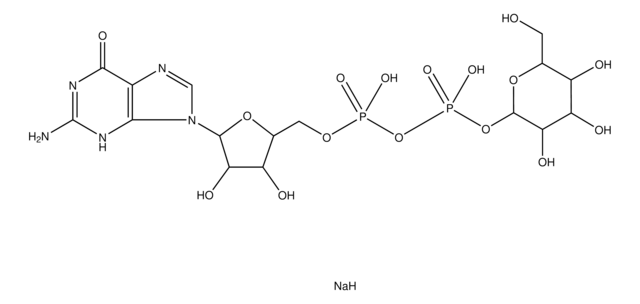
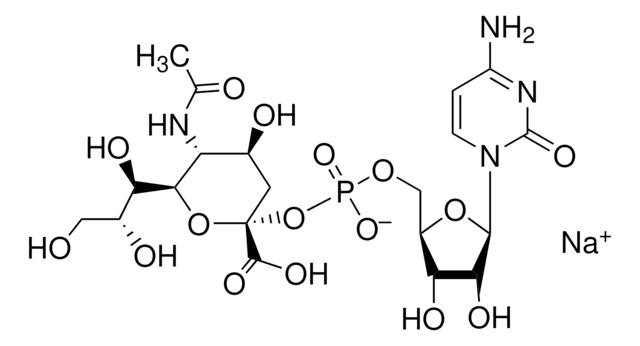
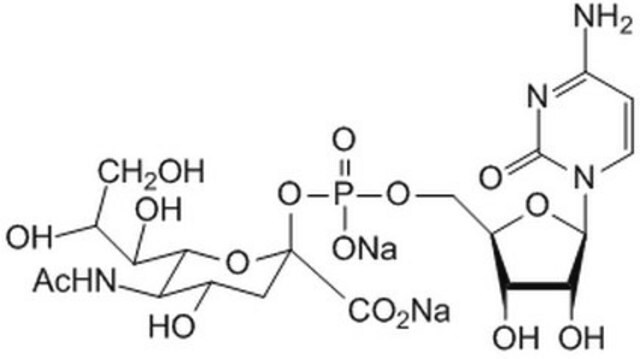
グアノシン 5′-ジホスホ-β-L-フコース ナトリウム塩, ≥85%
品質水準
アッセイ
≥85%
フォーム
powder
溶解性
water: 50 mg/mL, clear, colorless to faintly yellow
保管温度
−20°C
SMILES記法
CC1OC(OP(O)(=O)OP(O)(=O)OCC2OC(C(O)C2O)n3cnc4C(=O)N=C(N)Nc34)C(O)C(O)C1O
InChI
1S/C16H25N5O15P2/c1-4-7(22)9(24)11(26)15(33-4)35-38(30,31)36-37(28,29)32-2-5-8(23)10(25)14(34-5)21-3-18-6-12(21)19-16(17)20-13(6)27/h3-5,7-11,14-15,22-26H,2H2,1H3,(H,28,29)(H,30,31)(H3,17,19,20,27)
InChI Key
LQEBEXMHBLQMDB-UHFFFAOYSA-N
類似した製品をお探しですか? 訪問 製品比較ガイド
詳細
アプリケーション
基質
保管分類コード
11 - Combustible Solids
WGK
WGK 3
引火点(°F)
Not applicable
引火点(℃)
Not applicable
個人用保護具 (PPE)
Eyeshields, Gloves, type N95 (US)
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
G4401-VAR:
G4401-1MG:
G4401-2MG:
G4401-5MG:
G4401-BULK:
最新バージョンのいずれかを選択してください:
試験成績書(COA)
この製品を見ている人はこちらもチェック
資料
LC-MS/MS method quantifies similar polar nucleotide activated sugars using Supel™ Carbon LC column for simultaneous analysis.
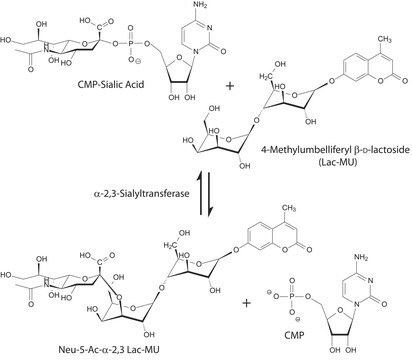
Explore tools for glycosyltransferase synthesis and modification of glycans, such as glycosyltransferases and nucleotide sugar donors.
Enzymatic glycosyltransferase specificity challenges the one enzyme-one linkage concept.
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)